Destiné au service des Affaires réglementaires,
-
gère les risques sur les dispositifs médicaux selon ISO 14971:2019
-
et génère automatiquement le Rapport de Gestion des Risques
RM 14971 est un module de la base de données Medical Device Software.
Un logiciel ISO 14971 intégrant les référentiels
Ce logiciel de management du risque selon ISO 14971 intègre du contenu issu de référentiels reconnus. Il s’appuie sur le contenu des normes ISO 14971, ISO 62304, ISO 62366, ISO 24971 ainsi que sur le guide pratique réalisé par les adhérents du SNITEM en collaboration avec le CETIM
Ainsi, vous y trouverez et pourrez utiliser pour mener vos analyses de risques des référentiels de dangers, d’évènements, de dommages sur l’homme, sur les équipements et sur l’environnement issus du guide CETIM et des normes en application associées.
Ce contenu est présent en français mais également en anglais.
Ces référentiels, qui sont contenus dans des bibliothèques, peuvent être modifiés/enrichis par les utilisateurs auxquels vous en donnerez l’autorisation. Vos référentiels spécifiques sont ainsi renseignés et capitalisés au fil de l’eau : situations dangereuses, actions à mener, etc.
La structure du logiciel et notamment des tableaux d’analyse des risques est définie en conformité avec l’ISO 14971:2019. Des références à cette norme sont présentes dans les en-têtes de colonnes (présence du numéro du chapitre de la norme associé à cette étape de l’analyse).
Grâce à la présence de ces référentiels, les utilisateurs sont guidés à travers la démarche et vous avez également la garantie d’être en conformité avec les normes applicables.
Différents éléments dans le logiciel vous guident pour vous aider à vérifier que vos évaluations sont conformes aux exigences de la norme. Un rapport spécifique est notamment dédié à cela : il reprend des chapitres essentiels de celle-ci et vous indique les lacunes éventuelles ou incohérences dans vos analyses de risque. Par exemple, s’il reste des bénéfices / risques non évalués, des risques combinés non pris en compte et réduits à leur tour, etc.
Risque sur les dispositifs médicaux selon ISO 14971
Dans le cadre de l’application de l’ISO 14971, vous devez avant de piloter vos analyses de risques préparer un certain nombre d’éléments. Le logiciel vous guidera dans les choix à faire pour définir votre organisation, la démarche, les règles d’évaluation que vous souhaiterez suivre et construire votre plan de gestion de risques.
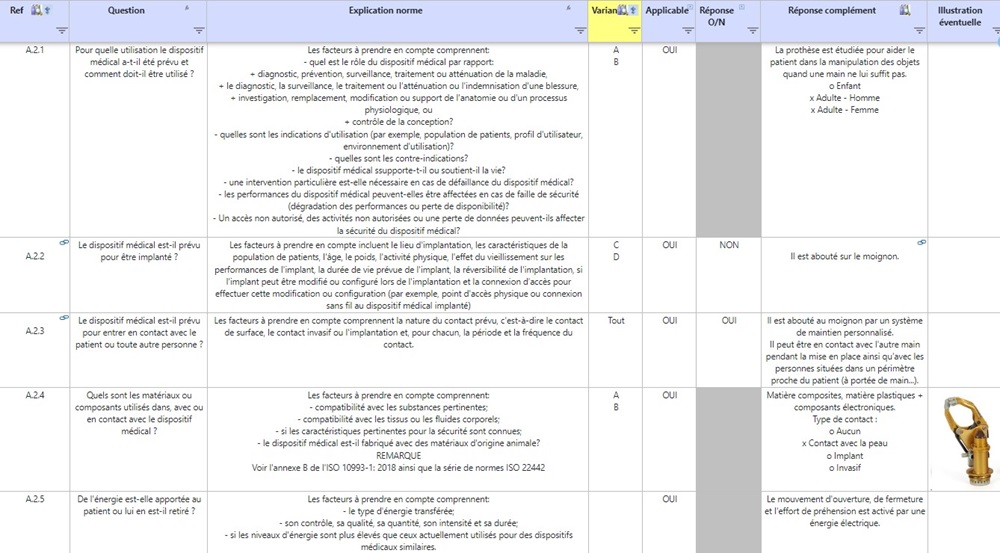
Un tableau vous permettra de répondre aux différentes questions permettant de décrire l’utilisation prévue du dispositif, en conformité avec l’ISO 14971. Cette analyse peut être réalisée pour chaque dispositif ou par famille de dispositif en indiquant les spécificités quand il y en a.
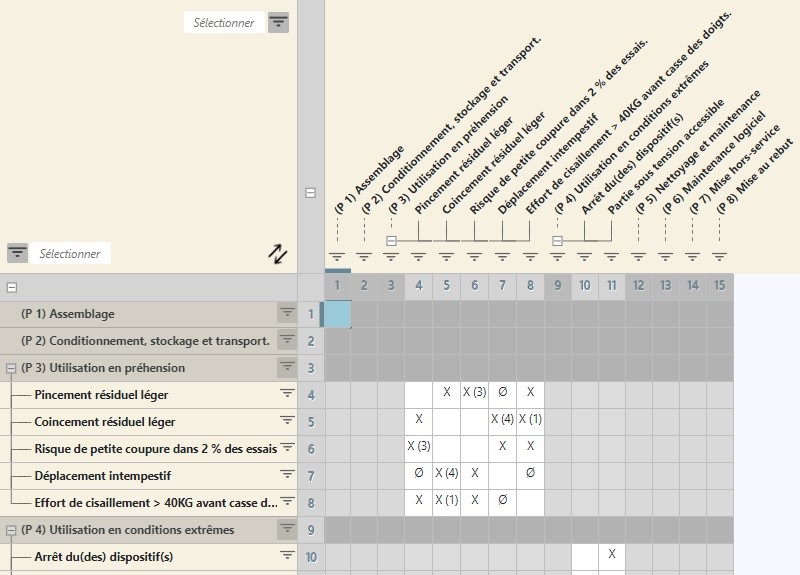
Le module RM14971 propose de dérouler l’analyse des risques en s’appuyant sur le cycle de vie du dispositif médical (DM) : conception, fabrication, transport, stockage, exploitation, maintenance, fin de vie, etc.
Il vous aide à identifier, analyser, et maîtriser les risques pour chacune de ces phases de vie.
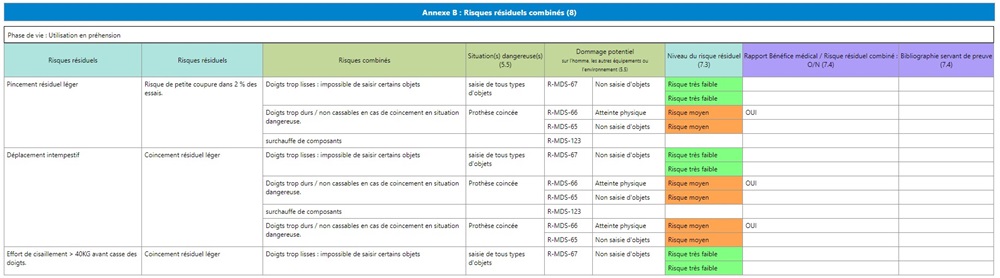
Afin de garantir la complétude de votre analyse, vous pouvez bien entendu prendre en considération de manière complète et facile les risques découlant des mesures ainsi que les risques résiduels combinés. Une matrice est à votre disposition pour identifier facilement les différentes combinaisons pertinentes des risques résiduels.
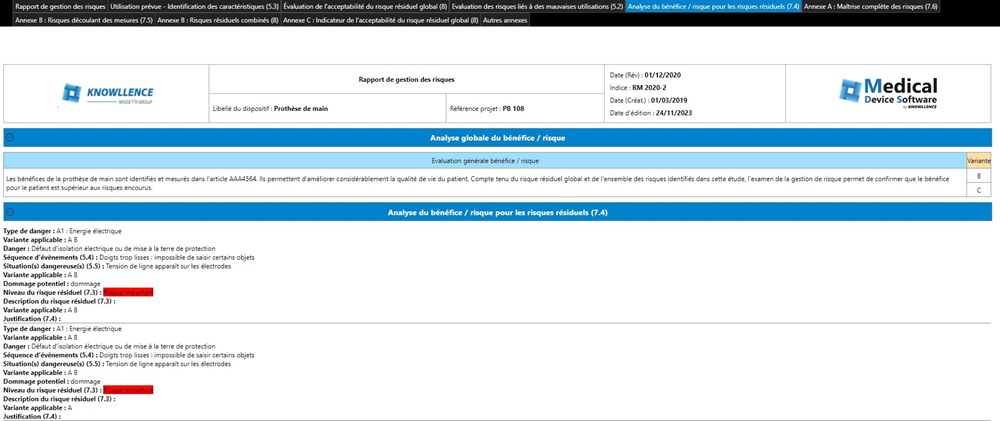
Conformément aux exigences de la norme, le logiciel permet ensuite de statuer pour chaque situation identifiée sur le bénéfice / risque puis sur l’acceptabilité du risque global au regard de ce risque.
Enfin, en conclusion de vos analyses de risques, vous pouvez renseigner les justifications associées au bénéfice / risque global ainsi qu’à l’acceptabilité globale associée au dispositif médical.
Les différentes revues de gestion de risques que vous effectuerez pourront être tracées dans le logiciel. Et les validations associées parfois à ces dernières seront également renseignées.
Un rapport dédié permettra de justifier en cas de besoin les différentes revues que vous aurez effectuées autour de votre projet.
Le rapport de gestion de risques s’édite ensuite automatiquement. Sa structure s’appuie sur les exigences de la norme.
Différents autres documents sont disponibles pour vous accompagner dans le pilotage efficace de votre démarche.
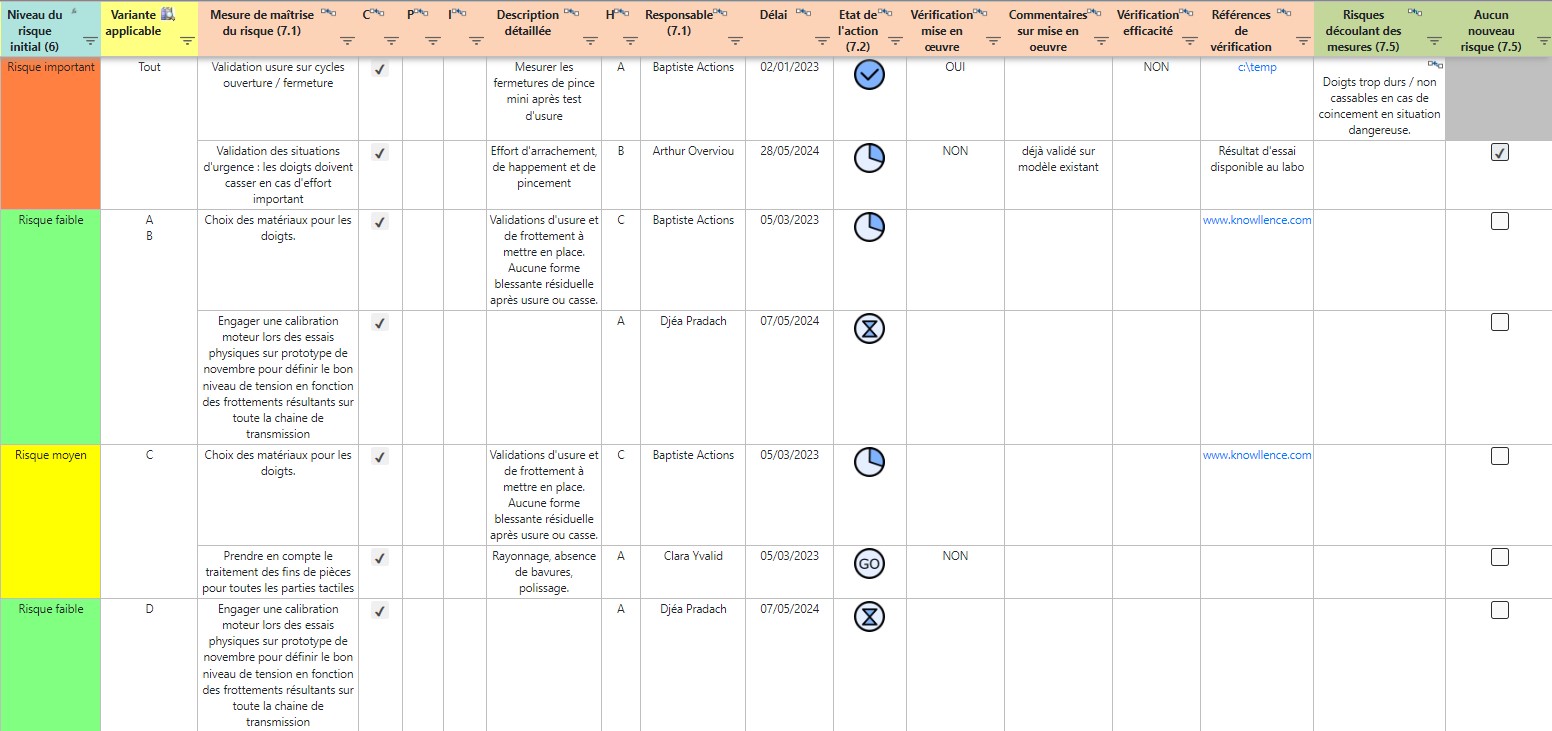
Prise en compte centralisée des actions de maîtrise des risques
Le module RM 14971 de Medical Device Suite permet de centraliser au sein de la même base le suivi des différents plans d’actions.
Les mesures de réduction des risques que vous proposerez peuvent être suivies en conformité avec les exigences de la norme. Les vérifications associées (mise en œuvre et efficacité) seront prises en compte ainsi que les catégories d’actions proposées (Conception, Protection, Information) et le niveau d’efficacité associé.
Un ensemble d’indicateurs et de reportings vous permettent de suivre l’avancement de ces actions, de piloter leur mise en œuvre. Une gestion globale des charges à l’ensemble des projets en cours est également intégrée dans Medical Device Suite.
Une analyse des risques intégrée dans votre Système de Management de la Qualité
Avec Medical Device Suite, votre analyse de risque 14971 n’est plus un outil utilisé de manière indépendante et séparé des autres analyses de risques (AMDEC Process par exemple) ou autres méthodes de votre cycle de conception / fabrication.
Des liens sont possibles entre les différentes étapes de votre démarche de conception afin de garantir une cohérence et une prise en compte des impacts liées aux modifications (notamment le post marché) efficace.
Il est ainsi possible, par exemple, de lier une situation dangereuse identifiée lors de l’analyse de risque 14971 avec une cause d’une AMDEC Process.
Un logiciel fourni avec son dossier de validation
Pour répondre aux principales exigences réglementaires et normatives des référentiels français, européens, nord-américains et internationaux, nous vous fournissons un logiciel qualifié et validé pour l’analyse de vos risques selon l’ISO 14971.
Aussi, nous élaborons et vous fournissons un dossier complet de validation à chaque sortie de version Medical Device Suite pour le module RM 14971.